医疗器械和药品同为医疗产品,由于产品的功能要求,有时需要将两者组合使用,称为药械组合产品。企业在药械组合产品研发和注册过程中,面临如何区分界定产品属性的问题。本文针对目前较常见的产品,解答如何区分产品是否属于医疗器械或药品。
1、药械组合产品的定义
药械组合产品系指由药品与医疗器械共同组成,并作为一个单一实体生产的医疗产品。以药品作用为主的药械组合产品,应当按照药品有关要求申报注册;以医疗器械作用为主的药械组合产品,应当按照医疗器械有关要求申报注册。
药械组合产品有药品和医疗器械两个属性,企业在注册产品时,需要明确产品的具体属性。可以通过查询《医疗器械分类目录》来确定属性,如目录中无该产品,则需要通过向国家药监局申请属性界定。
2、如何区分药械组合产品分类?
1)如何判断药械组合产品的属性?
企业研发药械组合产品前,可以通过申请属性界定来明确属性,或者用以下方法来预判断产品的属性:
a.先确定产品的预期用途,明确产品最基本的医疗功能;
b.将产品中的医疗器械部分去掉,判断产品能否实现该医疗功能;
c.将产品中的药品部分去掉,判断产品能否实现该医疗功能;
d.产品哪部分能实现基本的医疗功能(首要作用方式),产品大概率就属于该产品。
表1 药械组合产品属性判断举例
| 产品名称 | 基本医疗功能 | 药品部分功能 | 医疗器械部分功能 | 产品属性 |
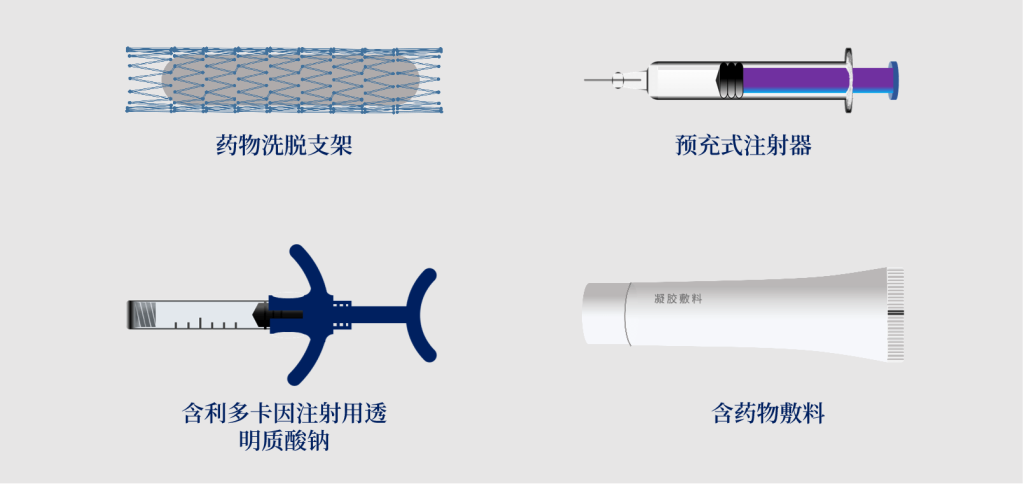
| 药物洗脱支架 | 血管支撑 | 抗增生作用 | 血管支撑 | 医疗器械 |
| 含利多卡因注射用透明质酸钠 | 组织填充 | 缓解疼痛 | 组织填充 | 医疗器械 |
| 预充式注射器 | 药物治疗 | 药物治疗 | 注射药物 | 药品 |
| 生长因子敷料 | 促进组织生长 | 促进组织生长 | 保湿 | 药品 |
2)属性界定
申请人通过药械组合产品属性界定信息系统向国家药监局标管中心提交药械组合产品属性界定申请。
属性界定资料包括:产品描述、作用机制、拟采用的使用说明书(或用户手册等)、组合产品各组成成分来源、申请人属性界定建议及论证资料、相关产品监管情况、其他与产品属性确定有关的资料
3)药械组合医疗器械成分
如企业希望药械组合产品按医疗器械注册,应尽量不采用用于特定症状治疗功能的药物成分。常见不建议采用的成分如下:
|
成分 |
组合器械 |
| 细胞因子 | 喷剂敷料、凝胶敷料、液体敷料、疤痕修复贴 |
| 多肽 | 喷剂敷料、凝胶敷料、液体敷料、疤痕修复贴 |
| 植物及其提取物 | 敷料、凝胶 |
| 中药 | 敷料、凝胶 |
3、注意事项
1)医疗器械属性的产品名称中不应体现“活性”二字。
2)医疗器械属性的产品预期用途中不应出现下列内容:“创面治疗”、“皮肤替代”、“生命支持”、“诱导组织”、“组织再生”。
3)药品和医疗器械需要配合使用,但产品分别独立包装,不属于药械组合产品。
